Семавик® Некст (семаглутид)
- Семавик® Некст — это препарат для похудения и поддержания массы тела, который содержит действующее вещество семаглутид.
- Семаглутид является аналогом глюкагоноподобного пептида 1 (ГПП-1) человека, который выделяется из кишечника после приема пищи. Семавик® Некст воздействует на рецепторы в головном мозге, которые контролируют аппетит, заставляя чувствовать себя сытым и менее голодным, а также испытывать меньшую тягу к еде. Это поможет есть меньше пищи и снизить массу тела. Семавик® Некст показан в качестве дополнения к низкокалорийной диете и физической нагрузке.
- Фармакологические концентрации семаглутида снижают концентрацию глюкозы крови и массу тела. Семаглутид оказывает положительное влияние на липиды плазмы крови, снижает систолическое артериальное давление и инсулинорезистентность
- Период полувыведения семаглутида (около 1 недели) позволяет применять его подкожно (п/к) 1 раз в неделю.
- Видео инструкция
- Механизм действия
- Краткая инструкция
- Особенности лекарственной формы
- Поиск по публикациям
Фармакодинамика
Все фармакодинамические исследования были проведены после 12 недель терапии (включая период увеличения дозы) в равновесной концентрации семаглутида 1 мг 1 раз в неделю.
Уровень гликемии натощак и постпрандиальный уровень гликемии
Семаглутид снижает концентрацию глюкозы натощак и концентрацию постпрандиальной глюкозы. По сравнению с плацебо терапия семаглутидом 1 мг у пациентов с сахарным диабетом 2 типа (СД2) привела к снижению концентрации глюкозы с точки зрения абсолютного изменения от исходного значения (ммоль/л) и относительного снижения по сравнению с плацебо (%) в отношении: концентрации глюкозы натощак (1,6 ммоль/л; 22%); концентрации глюкозы через 2 часа после приёма пищи (4,1 ммоль/л; 37%); средней суточной концентрации глюкозы (1,7 ммоль/л; 22%) и постпрандиальных пиков концентрации глюкозы за 3 приёма пищи (0,6-1,1 ммоль/л). Семаглутид снижал концентрацию глюкозы натощак после введения первой дозы.
Функция бета-клеток поджелудочной железы и секреция инсулина
Семаглутид улучшает функцию бета-клеток поджелудочной железы. После внутривенного струйного введения глюкозы пациентам с СД2 семаглутид по сравнению с плацебо улучшал первую и вторую фазу инсулинового ответа с трёхкратным и двукратным повышением, соответственно, и увеличивал максимальную секреторную активность бетаклеток поджелудочной железы после теста стимуляции аргинином. Кроме того, по сравнению с плацебо терапия семаглутидом увеличивает концентрации инсулина натощак.
Секреция глюкагона
Семаглутид снижает концентрацию глюкагона натощак и постпрандиальную концентрацию глюкагона. У пациентов с СД2 семаглутид приводит к относительному снижению концентрации глюкагона по сравнению с плацебо: концентрации глюкагона натощак (8-21%), постпрандиального глюкагонового ответа (14-15%) и средней суточной концентрации глюкагона (12%).
Глюкозозависимая секреция инсулина и глюкозозависимая секреция глюкагона
Семаглутид снижал высокую концентрацию глюкозы в крови, стимулируя секрецию инсулина и снижая секрецию глюкагона глюкозозависимым способом. Скорость секреции инсулина после введения семаглутида пациентам с СД2 была сопоставима с таковой у здоровых добровольцев.
Во время индуцированной гипогликемии семаглутид по сравнению с плацебо не изменял контррегуляторный ответ повышения концентрации глюкагона, а также не усугублял снижение концентрации С-пептида у пациентов с СД2.
Опорожнение желудка
Семаглутид вызывал небольшую задержку раннего постпрандиального опорожнения желудка, тем самым снижая скорость поступления постпрандиальной глюкозы в кровь.
Масса тела и состав тела
Наблюдалось большее снижение массы тела при применении семаглутида по сравнению с изученными препаратами сравнения (плацебо, ситаглиптином, эксенатидом замедленного высвобождения (ЗВ), дулаглутидом и инсулином гларгин) (см. раздел «Клиническая эффективность и безопасность»). Потеря массы тела при применении семаглутида происходила преимущественно за счёт потери жировой ткани, превышающей потерю мышечной массы в 3 раза.
Аппетит, потребление калорий и выбор продуктов питания
По сравнению с плацебо семаглутид снизил потребление калорий на 18-35 % во время трёх последовательных приёмов пищи ad libltum. Этому способствовали стимулированные семаглутидом подавление аппетита как натощак, так и после приёма пищи, улучшенный контроль потребления пищи, ослабление тяги к еде, особенно с высоким содержанием жиров.
Липиды натощак и постпрандиальные липиды
По сравнению с плацебо семаглутид снижал концентрации триглицеридов и холестерина липопротеинов очень низкой плотности (ЛПОНП) натощак на 12% и 21%, соответственно. Постпрандиальное увеличение концентрации триглицеридов и холестерина ЛПОНП в ответ на приём пищи с высоким содержанием жиров снизилось более чем на 40%.
Электрофизиология сердца (ЭФС)
Действие семаглутида на процесс реполяризации в сердце было протестировано в исследовании ЭФС. Применение семаглутида в дозах, превышающих терапевтические (в равновесной концентрации до 1,5 мг), не приводило к удлинению скорректированного интервала QТ.
Клиническая эффективность и безопасность
Как улучшение гликемического контроля, так и снижение СС заболеваемости и смертности являются неотъемлемой частью лечения СД2.
Эффективность и безопасность семаглутида в дозах 0,5 мг и 1 мг оценивались в шести рандомизированных контролируемых КИ За фазы. Из них пять КИ в качестве основной цели оценивали эффективность гликемического контроля, в то время как одно КИ оценивало в качестве основной цели СС исход. В дополнение были проведены два КИ семаглутида З фазы с участием японских пациентов.
В дополнение было проведено исследование Зb фазы для сравнения эффективности и безопасности семаглутида в дозах 0,5 мг и 1 мг один раз в неделю с дулаглутидом 0,75 мг и 1,5 мг один раз в неделю, соответственно. Также было проведено КИ Зb фазы с целью изучения эффективности и безопасности семаглутида в качестве дополнения к лечению ингибитором натрийзависимого переносчика глюкозы 2 типа (SGLТ2).
Терапия семаглутидом продемонстрировала устойчивые, статистически превосходящие и клинически значимые улучшение показателя НЬА1с и снижение массы тела на срок до 2 лет по сравнению с плацебо и лечением с активным контролем (ситаглиптином, инсулином гларгин, эксенатидом ЗВ и дулаглутидом).
Возраст, пол, раса, этническая принадлежность, исходные значения индекса массы тела (ИМТ) и массы тела (кг), длительность сахарного диабета (СД) и почечная недостаточность не повлияли на эффективность семаглутида.
Монотерапия
Монотерапия семаглутидом в дозах 0,5 мг и 1 мг 1 раз в неделю в течение 30 недель по сравнению с плацебо привела к статистически более значимому снижению показателей НЬА1с (-1,5%, -1,6% против 0%, соответственно), глюкозы плазмы натощак (ГПН) (-2,5 ммоль/л, -2,3 ммоль/л против -0,6 ммоль/л, соответственно) и массы тела (-3,7 кг, -4,5 кг против -1,0 кг, соответственно).
Семаглутид по сравнению с ситаглиптином, оба в комбинации с 1-2 пероральными гипогликемическими препаратами (ПГГП2) (метформином и/или препаратами группы тиазолидиндиона)
Терапия семаглутидом 0,5 мг и 1 мг 1 раз в неделю в течение 56 недель по сравнению с ситаглиптином привела к устойчивому и статистически более значимому снижению показателей НЬА1с (-1,3%, -1,6% против -0,5%, соответственно), ГПН (-2,1 ммоль/л, -2,6 ммоль/л против -1,1 ммоль/л, соответственно) и массы тела (-4,3 кг, -6,1 кг против -1,9 кг, соответственно). Терапия семаглутидом 0,5 мг и 1 мг по сравнению с ситаглиптином значительно снижала систолическое АД от исходного значения в 132,6 мм рт.ст. (-5,1 мм рт.ст., -5,6 мм рт.ст. против -2,3 мм рт.ст., соответственно). Изменений диастолического АД не происходило.
Семаглутид по сравнению с дулаглутидом, оба в комбинации с метформином
Терапия семаглутидом 0,5 мг по сравнению с дулаглутидом 0,75 мг, оба 1 раз в неделю на протяжении 40 недель, привела к устойчивому и статистически превосходящему снижению показателей НЬА1с (-1,5% против -1,1%), ГПН (-2,2 ммоль/л против -1,9 ммоль/л) и массы тела (-4,6 кг против -2,3 кг), соответственно.
Терапия семаглутидом 1 мг по сравнению с дулаглутидом 1,5 мг, оба 1 раз в неделю на протяжении 40 недель, привела к устойчивому и статистически превосходящему снижению показателей HbA1c (-l,8% против -1,4%), ГПН ( -2,8 ммоль/л против -2,2 ммоль/л) и массы тела (-6,5 кг против -3,0 кг), соответственно.
Семаглутид по сравнению с эксенатидом ЗВ, оба в комбинации с метформином или метформином совместно с производным сульфонилмочевины
Терапия семаглутидом 1 мг 1 раз в неделю на протяжении 56 недель по сравнению с эксенатидом ЗВ 2,0 мг привела к устойчивому и статистически более значимому снижению показателей НЬА1с (-1,5% против -0,9%), ГПН (-2,8 ммоль/л против -2,0 ммоль/л) и массы тела (-5,6 кг против -1,9 кг), соответственно.
Семаглутид по сравнению с инсулином гларгин, оба в комбинации с 1-2 ПГГП (монотерапия метформином или метформин с производным сульфонилмочевины)
Терапия семаглутидом в дозах 0,5 мг и 1 мг 1 раз в неделю по сравнению с инсулином гларгин в течение 30 недель привела к статистически более значимому снижению показателей НЬА1с (-1,2%, -1,6% против -0,8%, соответственно) и массы тела (-3,5 кг, -5,2 кг против +1,2 кг, соответственно).
Снижение показателя ГПН было статистически более значимым для семаглутида 1 мг по сравнению с инсулином гларгин (-2,7 ммоль/л против - 2,1 ммоль/л). Не наблюдалось статистически более значимое снижение показателя ГПН для семаглутида 0,5 мг (-2,0 ммоль/л против -2,1 ммоль/л). Доля пациентов, у которых наблюдались тяжёлые или подтверждённые (<3,1 ммоль/л) эпизоды гипогликемии, была ниже при применении семаглутида 0,5 мг (4,4%) и семаглутида 1 мг (5,6%) по сравнению с инсулином гларгин (10,6%).
Больше пациентов достигли показателя НЬА1с <7% без тяжёлых или подтверждённых эпизодов гипогликемии и без набора веса при применении семаглутида 0,5 мг (47%) и семаглутида 1 мг (64%) по сравнению с инсулином гларгин (16%).
Семаглутид по сравнению с плацебо, оба в комбинации с базальным инсулином
Терапия семаглутидом в дозах 0,5 мг и 1 мг по сравнению с плацебо в течение 30 недель привела к статистически более значимому снижению показателей НЬА1с (-1,4%, -1,8% против -0,1%, соответственно), ГПН ( -1,6 ммоль/л, -2,4 ммоль/л против -0,5 ммоль/л, соответственно) и массы тела (-3,7 кг, -6,4 кг против -1,4 кг, соответственно). Частота тяжёлых или подтверждённых эпизодов гипогликемии существенно не различалась при применении семаглутида и плацебо. Доля пациентов с показателем НЬА1с ≤8% на скрининге, сообщивших о тяжёлых или подтверждённых (<3,1 ммоль/л) эпизодах гипогликемии, была выше при применении семаглутида по сравнению с плацебо и сопоставима у пациентов с показателем НЬА1с >8% на скрининге.
Семаглутид по сравнению с плацебо в качестве дополнения к терапии ингибитором SGLT2 (в качестве монотерапии или в комбинации с производным сульфонилмочевины или метформином)
Терапия семаглутидом в дозе 1 мг раз в неделю в качестве дополнения к терапии ингибитором SGLТ2 (в качестве монотерапии или в комбинации с производным сульфонилмочевины или метформином) по сравнению с плацебо раз в неделю в течение 30 недель привела к статистически значимому снижению показателей НЬА1с (-1,5% против -0,1%, соответственно), ГПН (-2,2 ммоль/л против 0 ммоль/л, соответственно) и массы тела (-4,7 кг против -0,9 кг, соответственно).
Комбинация с монотерапией производным сульфонилмочевины
На 30-й неделе КИ (см. подраздел «Оценка влияния на ССС») была произведена оценка подгруппы из 123 пациентов, находящихся на монотерапии производным сульфонилмочевины. На 30-й неделе показатель НЬА1с снизился на 1,6% и на 1,5% при применении семаглутида в дозах 0,5 мг и 1 мг, соответственно, и увеличился на 0,1% при применении плацебо.
Комбинация с предварительно смешанным инсулином ± 1-2 ПГГП
На 30-й неделе КИ (см. подраздел «Оценка влияния на ССС») была произведена оценка подгруппы из 867 пациентов, находящихся на терапии предварительно смешанным инсулином (в комбинации или без 2-х ПГГП). На 30-й неделе показатель НЬА1с снизился на 1,3% и на 1,8% при применении семаглутида в дозах 0,5 мг и 1 мг, соответственно, и снизился на 0,4% при применении плацебо.
Соотношение пациентов, достигших целевого снижения показателя НЬА1с
До 79% пациентов достигли целей лечения в отношении снижения показателя НЬА1с <7%, и доля таких пациентов была значительно больше при применении семаглутида по сравнению с пациентами, получавшими ситаглиптин, эксенатид ЗВ, инсулин гларгин, дулаглутид и плацебо.
Доля пациентов, достигших показателя НЬА1с менее 7% без тяжёлых или подтверждённых эпизодов гипогликемии и без набора веса, была значительно больше при применении семаглутида в дозах 0,5 мг и 1 мг (до 66% и 74%, соответственно) по сравнению с пациентами, получавшими ситаглиптин (27%), эксенатид ЗВ (29%), инсулин гларгин (16%), дулаглутид 0,75 мг (44%) и дулаглутид 1,5 мг (58%).
Масса тела
Монотерапия семаглутидом 1 мг или терапия в комбинации с 1-2 лекарственными препаратами приводила к статистически большему снижению массы тела (потеря составляла до 6,5 кг) по сравнению с терапией плацебо, ситаглиптином, эксенатидом ЗВ, инсулином гларгин или дулаглутидом. Снижение массы тела было устойчивым на срок до 2-х лет.
После одного года терапии потери массы ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 0,5 мг (46% и 13%) и 1 мг (до 62% и 24%), по сравнению с пациентами, находившимися на терапии активными препаратами сравнения ситаглиптином и эксенатидом ЗВ (до 18% и до 4%).
В КИ длительностью 40 недель потери массы ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 0,5 мг (44% и 14%), по сравнению с пациентами, получавшими дулаглутид 0,75 мг (23% и 3%). Потери массы ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 1 мг (до 63% и 27%), по сравнению с пациентами, получавшими дулаглутид 1,5 мг (30% и 8%).
В СС КИ потери массы тела ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 0,5 мг (36% и 13%) и 1 мг (47% и 20%), по сравнению с пациентами, получавшими плацебо 0,5 мг (18% и 6%) и 1 мг (19% и 7%).
ГПН и постпрандиальное увеличение концентрации глюкозы
Во время всех трёх ежедневных приёмов пищи семаглутид 0,5 мг и 1 мг показал значительное снижение концентрации ГПН до 2,8 ммоль/л и снижение постпрандиального прироста концентрации глюкозы до 1,2 ммоль/л (разница между значениями до и после еды, полученная после трёх приёмов пищи) (в дополнение см. раздел «Фармакодинамика»).
Функция бета-клеток поджелудочной железы и инсулинорезистентность
В ходе терапии семаглутидом 0,5 мг и 1 мг произошло улучшение функции бета-клеток поджелудочной железы и уменьшение инсулинорезистентности, что подтверждается оценкой гомеостатических моделей функции бета-клеток поджелудочной железы (НОМА-В) и инсулинорезистентности (HOMA-IR) (в дополнение см. раздел «Фармакодинамика»).
Липиды
Во время КИ семаглутида наблюдалось улучшение профиля липидов крови натощак, преимущественно в группе, получавшей дозу 1 мг (в дополнение см. раздел «Фармакодинамика»).
Оценка влияния на ССС
3297 пациентов с СД2 и высоким СС риском были рандомизированы в двойное слепое КИ длительностью 104 недели на получение семаглутида 0,5 мг или 1 мг 1 раз в неделю либо плацебо 0,5 мг или 1 мг в дополнение к стандартной терапии СС заболеваний в течение последующих двух лет.
Терапия семаглутидом привела к снижению на 26% риска первичного комбинированного исхода, включающего смерть по причине СС патологии, инфаркт миокарда (ИМ) без смертельного исхода и инсульт без смертельного исхода. В первую очередь это было обусловлено значительным уменьшением частоты инсульта без смертельного исхода (39%) и незначительным уменьшением частоты ИМ без смертельного исхода (26%), но без изменений в частоте смерти по причине СС патологии.
Значительно снизился риск реваскуляризации миокарда или периферических артерий, в то время как риск нестабильной стенокардии, требующей госпитализации, и риск госпитализации по причине сердечной недостаточности снизились незначительно. Микроциркуляторные исходы включали в себя 158 новых или ухудшившихся случаев нефропатии. Относительный риск в отношении времени до возникновения нефропатии (новые случаи развития персистирующей макроальбуминурии, персистирующее удвоение сывороточной концентрации креатинина, необходимость в постоянной заместительной почечной терапии и смерть по причине болезни почек) составил 0,64.
В дополнение к стандартной терапии СС заболеваний терапия семаглутидом в дозах 0,5 мг и 1 мг по сравнению с плацебо 0,5 мг и 1 мг в течение 104 недель привела к значительному и устойчивому снижению от исходных значений показателя HbA1c (-1,1% и -1,4% против -0,4% и -0,4%, соответственно).
Артериальное давление
Наблюдалось значительное снижение среднего систолического АД при применении семаглутида 0,5 мг (3,5-5,1 мм рт.ст.) и семаглутида 1 мг (5,4-7,3 мм рт.ст.) в комбинации с ПГГП или базальным инсулином. Не отмечалось значительной разницы по показателям диастолического АД между семаглутидом и препаратами сравнения.
Листок-вкладыш - информация для пациента
Семавик® Некст, 0,25 мг/доза, раствор для подкожного введения Семавик® Некст, 0,5 мг/доза, раствор для подкожного введения Семавик® Некст, 1 мг/доза, раствор для подкожного введения Семавик® Некст, 1,7 мг/доза, раствор для подкожного введения Семавик® Некст, 2,4 мг/доза, раствор для подкожного введения Действующее вещество: семаглутид
Лекарственный препарат подлежит дополнительному мониторингу, который способствует быстрому выявлению новых сведений о безопасности. Вы можете помочь, сообщая информацию о любых нежелательных реакциях, которые возникли в период применения лекарственного препарата (в том числе и о случаях его неэффективности). Способ сообщения о нежелательных реакциях описан в разделе 4 листка-вкладыша.
Перед применением препарата полностью прочитайте листок-вкладыш, поскольку в нем содержатся важные для Вас сведения. Сохраните листок-вкладыш. Возможно, Вам потребуется прочитать его еще раз.
Если у Вас возникли дополнительные вопросы, обратитесь к лечащему врачу.
Препарат назначен именно Вам. Не передавайте его другим людям. Он может навредить им, даже если симптомы их заболевания совпадают с Вашими.
Если у Вас возникли какие-либо нежелательные реакции, обратитесь к лечащему врачу. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в разделе 4 листка-вкладыша.
Содержание листка-вкладыша:
- Что из себя представляет препарат Семавик® Некст и для чего его применяют.
- О чем следует знать перед применением препарата Семавик® Некст.
- Применение препарата Семавик® Некст.
- Возможные нежелательные реакции.
- Хранение препарата Семавик® Некст.
- Содержимое упаковки и прочие сведения.
Что из себя представляет препарат Семавик® Некст и для чего его применяют
Семавик® Некст — это препарат для похудения и поддержания массы тела, который содержит действующее вещество семаглутид. Семаглутид является аналогом глюкагоноподобного пептида 1 (ГПП-1) человека, который выделяется из кишечника после приема пищи. Семавик® Некст воздействует на рецепторы в головном мозге, которые контролируют ваш аппетит, заставляя Вас чувствовать себя сытым и менее голодным, а также испытывать меньшую тягу к еде. Это поможет Вам есть меньше пищи и снизить массу тела. Семавик® Некст показан в качестве дополнения к низкокалорийной диете и физической нагрузке.
Показания к применению
Препарат Семавик Некст показан к применению у взрослых в возрасте от 18 лет в дополнение к низкокалорийной диете и физической нагрузке для контроля массы тела,
включая снижение и поддержание массы тела, у взрослых с исходным индексом массы тела (ИМТ), равным:
- ≥ 30 кг/м2 (ожирение), или
- ≥ 27 кг/м2, но <30 кг/м2 (повышенная масса тела) при наличии по крайней мере одной сопутствующей патологии, связанной с массой тела, например дисгликемии (предиабет или сахарный диабет 2 типа (СД2)), артериальной гипертензии, дислипидемии, обструктивного апноэ во сне или сердечно-сосудистых заболеваний.
Препарат Семавик Некст показан к применению у взрослых от 18 лет с установленным сердечно-сосудистым заболеванием и ожирением или избыточной массой тела для снижения риска развития больших сердечно-сосудистых событий*
*большие сердечно-сосудистые события включают: смерть по причине сердечно- сосудистой патологии, инфаркт миокарда без смертельного исхода, инсульт без смертельного исхода.
Если улучшение не наступило или Вы чувствуете, необходимо обратиться к врачу.
Противопоказания
О чем следует знать перед применением препарата Семавик® Некст
Не применяйте препарат Семавик ® Некст если у Вас:
- гиперчувствительность к семаглутиду или любому из вспомогательных веществ, входящих в состав препарата и перечисленных в разделе 6;
- медуллярный рак щитовидной железы в анамнезе, в том числе в семейном;
- множественная эндокринная неоплазия (МЭН) 2 типа;
- сахарный диабет 1 типа (СД1); диабетический кетоацидоз;
- печёночная недостаточность тяжёлой степени;
- терминальная стадия почечной недостаточности (клиренс креатинина (КК) <15 мл/мин);
- хроническая сердечная недостаточность (ХСН) IV функционального класса (в соответствии с классификацией NУНА (Нью-Йоркская кардиологическая ассоциация)).
Особые указания и меры предосторожности
Перед применением препарата Семавик® Некст проконсультируйтесь с лечащим врачом.
Обязательно предупредите Вашего лечащего врача, если что-либо из нижеуказанных пунктов относится к Вам:
- Если в у Вас нарушения со стороны желудочно-кишечного тракта
Во время лечения препаратом Семавик® Некст у Вас могут появиться нежелательные реакции со стороны желудочно-кишечного тракта (ЖКТ), такие как тошнота, рвота или диарея, которые могут вызвать обезвоживание (потерю жидкости), что в редких случаях может привести к ухудшению функции почек. Важно, чтобы Вы пили достаточное количество жидкости, чтобы предотвратить обезвоживание. Это особенно важно, если у Вас проблемы с почками. - Если у Вас ранее был панкреатит (воспаление поджелудочной железы)
- Если у Вас появились сильная и продолжающаяся боль в животе, изжога, тошнота или рвота, ухудшение общего состояния немедленно обратитесь к врачу, так как это может быть признаком острого панкреатита (воспаления поджелудочной железы).
- Если у Вас появились признаки холецистита (воспаление желчного пузыря) – боль в правом подреберье, которая может отдавать в плечо, лопатку или ключицу, тошнота, отрыжка, появление желтушности склер или кожи, зуд кожи.
- Если у Вас сахарный диабет 2 типа
Семавик® Некст не является заменой инсулина.
Не применяйте препарат Семавик® Некст в комбинации с другими агонистами рецепторов ГПП-1, так как это может привести к усилению нежелательных реакций и передозировке. - Если Вы принимаете производные сульфонилмочевины или препараты инсулина. Комбинация этих препаратов с препаратом Семавик® Некст может увеличить риск снижения уровня сахара в крови (гипогликемии). Вам может потребоваться снижение дозы препаратов сульфонилмочевины или инсулина, проконсультируйтесь с лечащим врачом.
- Если у Вас диабетическая ретинопатия (диабетическая болезнь глаз)
Быстрое улучшение контроля уровня сахара в крови может привести к временному обострению диабетического заболевания глаз. Если Вы испытываете проблемы со зрением, проконсультируйтесь со своим врачом.
Не рекомендовано применение препарата Семавик® Некст, если у Вас следующие состояния/заболевания в связи с отсутствием данных по эффективности и безопасности или ограниченным опытом применения:
- применение других препаратов для снижения массы тела;
- сахарный диабет 1 типа;
- печеночная недостаточность тяжелой степени;
- терминальная стадия почечной недостаточности;
- хроническая сердечная недостаточность (ХСН) IV функционального класса (в соответствии с классификацией NYHA).
С осторожностью применяйте препарат Семавик® Некст если у Вас:
- возраст старше 75 лет;
- легкая или умеренная печеночная недостаточность;
- воспалительные заболевания кишечника;
- диабетический парез желудка.
Риск аспирации или аспирационной пневмонии
При проведении оперативных вмешательств под общей анестезией или глубокой седацией у пациентов, получающих агонисты ГПП-1, возможен риск развития аспирации или аспирационной пневмонии из-за задержки опорожнения желудка и присутствия остаточного желудочного содержимого.
Другие препараты и Семавик® Некст
Сообщите Вашему лечащему врачу, если Вы принимаете, недавно принимали или можете начать принимать какие-либо другие препараты.
Сообщите Вашему врачу, если вы принимаете препараты, содержащие варфарин или другие подобные лекарства, для снижения свертываемости крови (пероральные антикоагулянты). Вам может потребоваться частый анализ крови для определения способности крови свертываться.
Беременность и грудное вскармливание
Не применяйте препарата Семавик® Некст во время беременности, так как неизвестно, может ли препарат повлиять на Вашего будущего ребенка.
Используйте надежные средства контрацепции в период применения препарата Семавик® Некст.
Если Вы хотите забеременеть, Вам следует прекратить прием препарата Семавик® Некст по крайней мере за два месяца до планируемой беременности.
Если Вы забеременели или думаете, что можете забеременеть, или планируете завести ребенка в период применения препарата Семавик® Некст, немедленно проконсультируйтесь с лечащим врачом, поскольку Ваше лечение препаратом Семавик® Некст нужно будет прекратить.
Не применяйте препарат Семавик® Некст, если Вы кормите грудью, поскольку неизвестно, проникает ли препарат в грудное молоко человека.
Управление транспортными средствами и работа с механизмами
Семавик® Некст не повлияет на Вашу способность управлять транспортными средствами и пользоваться механизмами. Однако некоторые пациенты могут испытывать головокружение при применении препарата Семавик® Некст в течение первых 4 месяцев лечения (см. раздел «Возможные нежелательные реакции»). Если Вы чувствуете головокружение, Вам не следует садиться за руль или работать с механизмами, пока Вы не почувствуете себя лучше. Если Вам нужна какая-либо дополнительная информация, обратитесь к своему лечащему врачу.
Если у Вас СД2, то при применении препарата Семавик® Некст в комбинации с препаратами производными сульфонилмочевины или инсулином, может снизиться уровень сахара в крови (гипогликемия), что может ослабить способность концентрироваться. Не садитесь за руль или не пользуйтесь механизмами, если у Вас появились какие-либо признаки гипогликемии (см. раздел "Особые указания и меры предосторожности" для получения информации о повышенном риске снижения уровня сахара в крови и раздел 4 для получения предупреждающих признаков низкого уровня сахара в крови. Обратитесь к своему лечащему врачу за дополнительной информацией.
Прослеживаемость
Для улучшения прослеживаемости препарата необходимо записывать серии и срок годности партии введенного препарата.
Вспомогательные вещества
Препарат Семавик® Некст содержит менее 1 ммоль натрия (23 мг) на одну дозу (2,4 мг), то есть по сути не содержит натрия.
Применение препарата Семавик® Некст
Всегда применяйте препарат в полном соответствии с рекомендациями лечащего врача. При появлении сомнений посоветуйтесь с лечащим врачом.
Дозу и режим введения препарата подберет Ваш лечащий врач с учетом Ваших индивидуальных особенностей.
Рекомендуемая доза
Взрослые
Рекомендуемая начальная доза 0,5 мг один раз в неделю. Рекомендуемая терапевтическая доза 2,4 мг один раз в неделю.
Ваше лечение начнется с начальной дозы, которая будет постепенно увеличиваться в течение 16 недель лечения следующим образом:
- Ваш врач проинструктирует Вас постепенно увеличивать дозу каждые 4 недели, как указано в таблице ниже, пока вы не достигнете рекомендуемой терапевтической дозы 2,4 мг один раз в неделю.
- Как только Вы достигнете рекомендуемой дозы 2,4 мг, больше не увеличивайте эту дозу.
| Увеличение дозы | Еженедельная доза |
| Неделя 1-4 | 0,25 мг |
| Неделя 5-8 | 0,5 мг |
| Неделя 9-12 | 1 мг |
| Неделя 13-16 | 1,7 мг |
| Поддерживающая доза | 2,4 мг |
Еженедельные дозы, превышающие 2,4 мг, не рекомендуются. Ваш лечащий врач будет регулярно оценивать Ваше лечение.
Применение у детей и подростков
Эффективность и безопасность для детей не установлены.
Путь и способ введения
Препарат Семавик® Некст вводится в виде инъекции под кожу (подкожная инъекция) с помощью шприц-ручки. Никогда не вводите препарат Семавик® Некст в вену или в мышцу.
- Лучшими местами для инъекции являются предплечья, живот или верхняя часть бедер.
- Прежде чем использовать шприц-ручку в первый раз, спросите своего лечащего врача, как с ней обращаться. Внимательно прочитайте инструкцию по применению предварительно заполненной мультидозовой одноразовой шприц-ручки Семавик® Некст, вложенную в упаковку. Используйте шприц-ручку только в соответствии с инструкцией по ее применению.
- Всегда проверяйте, что вы используете нужную вам дозировку Семавик® Некст.
Вводите препарат Семавик® Некст один раз в неделю и, по возможности, в один и тот же день каждую неделю. При необходимости Вы можете изменить день еженедельной инъекции этого препарата, если с момента Вашей последней инъекции прошло не менее 3 дней. После выбора нового дня приема продолжайте принимать препарат один раз в неделю.
Вы можете делать себе инъекцию в любое время дня – независимо от приема пищи.
Пациенты с сахарным диабетом 2 типа
Сообщите своему лечащему врачу, если у Вас СД2. Ваш врач может скорректировать дозу препаратов, применяемых для лечения СД2, чтобы предотвратить снижение содержания сахара в крови.
- Не комбинируйте препарат Семавик® Некст с другими лекарственными средствами, которые Вы вводите подкожно (например, инсулинами).
- Не используйте препарат Семавик® Некст в комбинации с другими лекарственными средствами, содержащими агонисты рецепторов ГПП-1 (такими как лираглутид, дулаглутид, эксенатид или ликсисенатид).
Продолжительность терапии
Ваш врач будет регулярно оценивать Ваше состояние и скажет Вам, как долго следует применять препарат Семавик® Некст.
Если Вы применили препарат Семавик® Некст в большей дозе, чем требовалось
Немедленно обратитесь к Вашему лечащему врачу. У Вас могут возникнуть нежелательные реакции со стороны желудочно-кишечного тракта (ЖКТ), такие как тошнота, рвота или диарея. Это может привести к обезвоживанию, что в редких случаях может привести к ухудшению функции почек.
Если Вы забыли применить препарат Семавик® Некст
Если Вы забыли ввести дозу и:
- прошло 5 дней или менее с тех пор, как Вы должны были сделать инъекцию Семавик® Некст – введите пропущенную дозу, как только вспомните. Затем введите следующую дозу, как обычно, в назначенный день.
- прошло более 5 дней с тех пор, как Вы должны были сделать инъекцию Семавик® Некст – не вводите пропущенную дозу. Подождите и введите следующую дозу как обычно в запланированный день.
Никогда не вводите двойную дозу, чтобы восполнить пропущенную.
Если Вы прекратили применение препарата Семавик® Некст
Не прекращайте применение препарат Семавик® Некст без консультации с Вашим лечащим врачом. Если у Вас возникнут какие-либо дополнительные вопросы по применению препарата Семавик® Некст обратитесь к лечащему врачу.
Возможные нежелательные реакции
Подобно всем лекарственным препаратам, препарат Семавик® Некст может вызывать нежелательные реакции, но они возникают не у всех.
Наиболее серьезные нежелательные реакции
Прекратите применение препарата Семавик® Некст и немедленно обратитесь за медицинской помощью в случае возникновения одного из следующих признаков тяжелой аллергической реакции (анафилактические реакции, ангионевротический отек), которая наблюдалась редко (может возникать не более чем у 1 человека из 1000):
- затрудненное дыхание или глотание;
- головокружение;
- отек лица, губ, языка или горла;
- сильный зуд кожи, появление сыпи или волдырей;
- предобморочное состояние (падение кровяного давления) с учащенным сердцебиением и повышенным потоотделением.
- бледность и холод кожи, головокружение или слабость.
Если у Вас сахарный диабет 2 типа, сообщите своему лечащему врачу, если во время лечения препаратом Семавик® Некст у Вас возникнут проблемы со зрением, например, нарушение зрения, которое наблюдалось часто (может возникать не более чем у 1 человека из 10):
- Осложнения диабетической болезни глаз (диабетическая ретинопатия).
Немедленно обратитесь за медицинской помощью, если Вы испытываете симптомы воспаления поджелудочной железы (острый панкреатит), которое наблюдалось нечасто (встречаются не более чем у 1 из 100):
- сильная и продолжительная боль в животе, которая может отдавать в спину;
- внезапные интенсивные боли во всей брюшной полости;
- изжога;
- приступы рвоты;
- вздутие живота и метеоризм;
- ухудшение общего состояния: повышение температуры тела, снижение артериального давления, тахикардия, потливость, бледность или желтушность кожи.
Другие возможные нежелательные реакции, которые могут наблюдаться при применении препарата Семавик® Некст
Очень часто (встречается более чем у 1 человека из 10):
- Головная боль;
- Тошнота;
- Рвота;
- Диарея;
- Запор;
- Боль в животе;
- Чувство слабости или усталость.
Часто (встречается не более чем у 1 человека из 10):
- Головокружение;
- Дисгевзия
- Расстройство желудка или несварение желудка;
- Отрыжка;
- Метеоризм;
- Вздутие живота;
- Воспаление желудка ("гастрит") – признаки включают боль в животе, тошноту или рвоту;
- Рефлюкс или изжога, также называемая "гастроэзофагеальная рефлюксная болезнь";
- Желчнокаменная болезнь;
- Потеря волос;
- Реакции в месте введения;
- Снижение содержания сахара в крови (гипогликемия) у пациентов с сахарным диабетом*.
*Признаки снижения содержания сахара в крови могут проявиться внезапно. Они могут включать: холодный пот, прохладную бледную кожу, головную боль, учащенное сердцебиение, плохое самочувствие (тошноту) или сильный голод, изменения в зрении, сонливость или слабость, нервозность, беспокойство или растерянность, трудности с концентрацией внимания или дрожь. Ваш лечащий врач расскажет Вам, как повысить содержание сахара в крови и что делать, если Вы заметили эти предупреждающие признаки. Гипогликемия более вероятна, если Вы также принимаете препараты производные сульфонилмочевины или инсулин. Ваш врач может уменьшить дозу этих препаратов, прежде чем Вы начнете применять Семавик® Некст.
Нечасто (встречаются не более чем у 1 из 100):
- Учащение сердцебиения;
- Пониженное давление крови (гипотензия);
- Снижение артериального давления при переходе из горизонтального положения (сидячего или лежачего) в вертикальное (стоячее) (ортостатическая гипотензия);
- Повышение уровней липазы и амилазы в анализе крови;
- Задержка опорожнения желудка.
Редко (встречается не более чем у 1 человека из 1000):
- Кишечная непроходимость
- Холангит
- Холестатическая желтуха
Сообщите своему лечащему врачу, если у Вас появились какие-либо новые или ухудшились имеющиеся симптомы.
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке-вкладыше. Вы также можете сообщить о нежелательных реакциях напрямую через систему сообщений государств – членов Евразийского экономического союза. Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
Российская Федерация
Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор) Адрес: 109012, Москва, Славянская площадь, д. 4, стр. 1
Телефон: +7 800 550 99 03
Электронная почта: pharm@roszdravnadzor.gov.ru
Сайт в информационно-телекоммуникационной сети «Интернет»: www.roszdravnadzor.gov.ru
Хранение препарата Семавик® Некст
Храните препарат Семавик® Некст в недоступном для ребенка месте так, чтобы ребенок не мог увидеть его.
Не применяйте препарат Семавик® Некст после истечения срока годности (срока хранения), указанного на этикетке шприц-ручки и упаковке. Датой истечения срока годности является последний день данного месяца.
Храните препарат Семавик® Некст в холодильнике при температуре от 2 до 8 °C.
Не замораживайте, не размещайте рядом с морозильной камерой, не используйте, если препарат был заморожен.
После первого использования
Храните используемую или переносимую в качестве запасной шприц-ручку с препаратом при температуре не выше 30 °С или при температуре от 2 °С до 8 °С (в холодильнике) не более 6 недель.
Не замораживайте. После использования закрывайте шприц-ручку колпачком для защиты от света. Предохраняйте от воздействия избыточного тепла.
Не используйте препарат Семавик® Некст, если заметили, что раствор не прозрачный и бесцветный.
Не выбрасывайте (не выливайте) препарат в канализацию. Уточните у работника аптеки, как следует утилизировать (уничтожать) препарат, который больше не потребуется. Эти меры позволяют защитить окружающую среду.
Содержимое упаковки и прочие сведения Препарат Семавик® Некст содержит
Действующим веществом является семаглутид.
Семавик® Некст, 0,25 мг/доза, раствор для подкожного введения
Каждый мл раствора содержит 0,68 мг семаглутида. Каждая предварительно заполненная шприц-ручка содержит 2,04 мг семаглутида в 3 мл раствора (4 дозы по 0,25 мг).
Прочими ингредиентами являются: динатрия гидрофосфата дигидрат, пропиленгликоль, фенол, хлористоводородной кислота раствор 10% или натрия гидроксида раствор 10% (для коррекции pH), вода для инъекций.
Семавик® Некст, 0,5 мг/доза, раствор для подкожного введения
Каждый мл раствора содержит 1,34 мг семаглутида. Каждая предварительно заполненная шприц-ручка содержит 4 мг семаглутида в 3 мл раствора (8 доз по 0,5 мг).
Прочими ингредиентами являются: динатрия гидрофосфата дигидрат, пропиленгликоль, фенол, хлористоводородной кислота раствор 10% или натрия гидроксида раствор 10% (для коррекции pH), вода для инъекций.
Семавик® Некст, 1 мг/доза, раствор для подкожного введения
Каждый мл раствора содержит 1,34 мг семаглутида. Каждая предварительно заполненная шприц-ручка содержит 4 мг семаглутида в 3 мл раствора (4 дозы по 1 мг).
Прочими ингредиентами являются: динатрия гидрофосфата дигидрат, пропиленгликоль, фенол, хлористоводородной кислота раствор 10% или натрия гидроксида раствор 10% (для коррекции pH), вода для инъекций.
Семавик® Некст, 1,7 мг/доза, раствор для подкожного введения
Каждый мл раствора содержит 2,27 мг семаглутида. Каждая предварительно заполненная шприц-ручка содержит 6,8 мг семаглутида в 3 мл раствора (4 дозы по 1,7 мг).
Прочими ингредиентами являются: динатрия гидрофосфата дигидрат, пропиленгликоль, фенол, хлористоводородной кислота раствор 10% или натрия гидроксида раствор 10% (для коррекции pH), вода для инъекций.
Семавик® Некст, 2,4 мг/доза, раствор для подкожного введения
Каждый мл раствора содержит 3,2 мг семаглутида. Каждая предварительно заполненная шприц-ручка содержит 9,6 мг семаглутида в 3 мл раствора (4 дозы по 2,4 мг).
Прочими ингредиентами являются: динатрия гидрофосфата дигидрат, пропиленгликоль, фенол, хлористоводородной кислота раствор 10% или натрия гидроксида раствор 10% (для коррекции pH), вода для инъекций.
Препарат Семавик® Некст содержит натрий (см. раздел 2)
Внешний вид препарата Семавик® Некст и содержимое упаковки
Семавик® Некст раствор для подкожного введения представляет собой бесцветный или почти бесцветный прозрачный раствор.
По 3 мл в бесцветные стеклянные картриджи нейтрального стекла (1 гидролитический класс) с плунжерами резиновыми из бромбутилового каучука, обкатанные колпачками комбинированными из алюминия с дисками резиновыми из бромбутилового каучука.
Картридж устанавливают в пластиковую мультидозовую одноразовую шприц-ручку для многократных инъекций, позволяющую вносить дозы 0,25/ 0,5/ 1,0/ 1,7/ 2,4 мг/доза. На корпус каждой шприц-ручки наклеивают этикетку из пленки полипропиленовой.
По 1 предварительно заполненной мультидозовой одноразовой шприц-ручке для многократных инъекций и 1 пачке картонной, содержащей 4 одноразовых иглы, с листком- вкладышем, включающем инструкцию по использованию шприц-ручки, помещают в пачку из картона.
Держатель регистрационного удостоверения
Российская Федерация ООО «ГЕРОФАРМ»
191119, г. Санкт-Петербург, ул. Звенигородская, д. 9 Тел: +7 (812) 703 79 75 (многоканальный)
Факс: +7 (812) 703 79 76
Электронная почта: inform@geropharm.ru
Производитель Российская Федерация ООО «ГЕРОФАРМ»
- Московская обл., г.о. Серпухов, п. Оболенск, тер. Квартал А, стр. 5
- Московская обл., г.о. Серпухов, п. Оболенск, тер. Квартал А, к.1, стр. 5
- Московская обл., г.о. Серпухов, п. Оболенск, тер. Квартал А, к. 82, стр. 4
Все претензии потребителей следует направлять представителю держателя регистрационного удостоверения или держателю регистрационного удостоверения:
Российская Федерация ООО «ГЕРОФАРМ»
196608, г. Санкт-Петербург, г. Пушкин, Ячевский проезд, д.4, стр.1 Тел: +7 (812) 703 79 75
Факс: +7 (812) 703 79 76
Электронная почта: inform@geropharm.ru; farmakonadzor@geropharm.com
Листок-вкладыш пересмотрен:
Прочие источники информации
Подробные сведения о данном препарате содержатся на веб-сайте Союза https://eec.eaeunion.org/
ИНСТРУКЦИЯ ПО ИСПОЛЬЗОВАНИЮ ШПРИЦ-РУЧЕК
Пен-иньектор представляет собой предварительно заполненную одноразовую шприц-ручку для многократных инъекций (далее «Шприц-ручка»), содержащую гипогликемическое средство, аналог глюкагоноподобного пептида-1 (ГПП-1) – семаглутид.
Семавик® Некст (0,25 мг/доза, 0,5 мг/доза, 1 мг/доза, 1,7 мг/доза, 2,4 мг/доза) - раствор для п/к введения в предварительно заполненной шприц-ручке. Одна шприц-ручка содержит 3 мл раствора.
На каждой шприц-ручке Семавик®Некст можно выбрать только одну дозу: 0,25 мг, или 0,5 мг, или 1 мг, или 1,7 мг, или 2,4 мг.
Шприц-ручка предназначена для использования с одноразовыми инъекционными иглами WellFine, Dexfine и Verifine. В упаковку препарата Семавик® Некст включены иглы WellFine 4 mm 32G (Dexfine 4 mm 32G или Verifine 4 mm 32G) в количестве 4 шт.
Препарат Семавик® Некст можно вводить при помощи игл длиной до 8 мм.
Перед каждой инъекцией необходимо использовать новую иглу. После инъекции хранить и транспортировать шприц-ручку необходимо без иглы! Это предотвращает непроходимость игл, загрязнение, заражение, вытекание раствора и введение некорректной дозы препарата.
Утилизировать иглы необходимо согласно местным требованиям, соблюдая нормы и правила обращения с потенциально инфицированными материалами.
Применение шприц-ручки должно проводиться только одним человеком. Шприц-ручка не должна передаваться третьему лицу.
Если препарат Семавик®Некст в шприц-ручке выглядит иначе, чем бесцветный прозрачный раствор, то его применять нельзя.
Не подвергайте ручки воздействию низких (ниже +2°С) и высоких (выше +30°С) температур. Не помещайте шприц-ручки в морозильную камеру. Шприц-ручки нельзя замораживать!
Использованные шприц-ручки подлежат утилизации и не должны повторно эксплуатироваться (нельзя повторно заполнять шприц-ручку).
Транспортировать шприц-ручки при высоких/низких температурах воздуха лучше в специальном термопенале/сумке (например, оригинальный термопенал ГЕРОФАРМ).
Храните шприц-ручку и иглы в недоступных для всех, и в особенности для детей, местах.
Не пытайтесь самостоятельно ремонтировать шприц-ручку. В случае поломки сообщите в организацию, принимающую претензии потребителей, указанную в инструкции по медицинскому применению препарата. Телефон информационной линии помощи ГЕРОФАРМ: 8 (800) 333-43-76.
Инструкция по применению предварительно заполненной шприц-ручки с препаратом Семавик® Некст 0,25 мг/доза, 0,5 мг/доза, 1 мг/доза, 1,7 мг/доза, 2,4 мг/доза раствор для подкожного введения.
Перед первой инъекцией необходимо внимательно прочитать и изучить инструкцию по использованию предварительно заполненных одноразовых шприц-ручек.
Необходимо проконсультироваться с лечащим врачом (специалистом) по применению шприц-ручки. Попросите продемонстрировать правильное использование шприц-ручки. Первая инъекция препарата должна проводиться под контролем врача или медсестры.
Внимательно прочитайте этикетку на шприц-ручке и убедитесь в том, что Вы используете именно тот лекарственный препарат, который Вам назначил врач, в нужной Вам дозировке, а также проверьте срок годности препарата. Затем посмотрите на представленные ниже иллюстрации, чтобы ознакомиться с характеристиками и составными частями шприц-ручки.
Перед началом использования шприц-ручки необходимо исследовать ее на наличие видимых механических повреждений и подтеков (свидетельствующих о нарушении герметичности картриджа). Если Вы не уверены, что шприц-ручка исправна, и у нее отсутствуют повреждения, никогда не пользуйтесь шприц-ручкой. Всегда проверяйте шприц-ручку перед каждой инъекцией.
Тщательно следуйте инструкции по использованию шприц-ручки: предотвращайте падение ручки и влияние прочих внешних факторов (термальное воздействие, прямые солнечные лучи, механическое повреждение и пр.). Если произошло повреждение, необходимо начать использовать новую шприц-ручку.
Слабовидящий пациент или пациент, у которого имеются серьезные проблемы со зрением, и он не может различить цифры на счетчике дозы, должен использовать шприц-ручку под контролем медицинского персонала, родственников или человека с хорошим зрением, прошедших обучение по введению препарата предварительно заполненной шприц-ручкой.
Лица, осуществляющие уход за больным, должны обращаться с использованными иглами с особой осторожностью, чтобы предотвратить уколы иглой и перекрестное инфицирование.
Предварительно заполненная шприц-ручка с препаратом Семавик® Некст
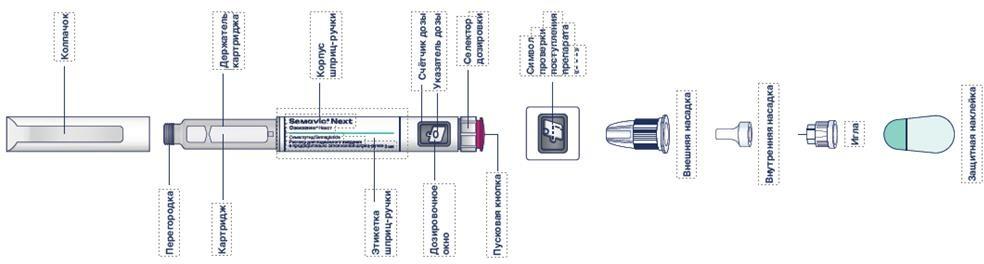
Внешний вид предварительно заполненной шприц-ручки
| I. Подготовка шприц-ручки с новой иглой к использованию | |
| 1. Проверьте название на этикетке шприц-ручки. Необходимо убедиться, что в ручке содержится препарат Семавик® Некст 0,25 мг/доза, 0,5 мг/доза, 1 мг/доза, 1,7 мг/доза, 2,4 мг/доза. Это особенно важно, если Вы применяете более одного инъекционного препарата. |

|
|
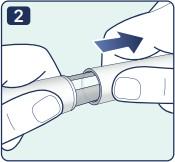
2. Удерживайте шприц-ручку одной рукой и снимите колпачок со шприц- ручки, потянув за него другой рукой. |
| 3. Убедитесь, что раствор в шприц- ручке бесцветный или почти бесцветный и прозрачный. Посмотрите в окошко держателя картриджа шприц-ручки. Примечание: Если раствор мутный, не бесцветный или есть посторонние примеси,такуюшприц-ручку использовать нельзя! | 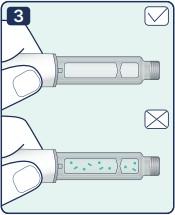
|

|
4. Возьмите новую иглу и удалите защитную наклейку с внешней насадки иглы. Примечание: Используйте иглы строго в соответствии с рекомендациями врача. При каждой инъекции используйте новую иглу, чтобы свести к минимуму риск введения неправильной дозы препарата, инфицирования и травматизации тканей. |
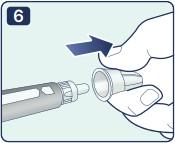
| 5. При помощи внешней насадки иглы установите ее точно на держатель картриджа. Надежно закрутите ее, чтобы игла плотно держалась на шприц-ручке. | 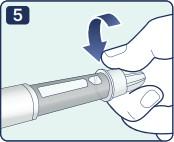
|
|
6. Снимите наружный колпачок иглы, но не выбрасывайте его. Он понадобится после завершения инъекции, чтобы безопасно снять иглу со шприц-ручки. |
| 7. Снимите Внутреннюю насадку и выбросите. Удерживайте шприц-ручку иглой вверх. Слегка постучите пальцем по держателю картриджа, чтобы пузырьки воздуха поднялись вверх. Наличие мелкодисперсных пузырьков допустимо. Примечание: Игла становится видимой (обнажается) помере удаления внутренней насадки. | 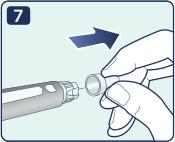
|
| При установке иглы на держатель картриджа может появиться капля препарата, это нормальное явление, однако все равно необходимо проверить прохождение (поступление) препарата через иглу, если шприц-ручка используется в первый раз. Присоединяйте новую иглу к шприц-ручке непосредственно перед инъекцией, когда пациент будет готов к введению препарата. | |
| II. Проверка прохождения (поступления) препарата через иглу | |
|
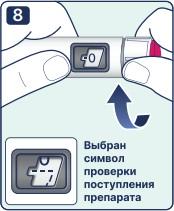
8. Перед первым применением шприц-ручки необходимо проверить прохождение (поступление) препарата через иглу. Прокрутите селектор дозировки до символа проверки прохождения (поступления) препарата таким образом, чтобы символ совпадал с указателем дозы. При наборе символа проверки вы должны услышать 2 (два) щелчка. Примечание: Если селектор дозировки проскочил необходимый символ, прокрутите его в противоположном направлении для того, чтобы скорректировать положение символа проверки. Если шприц-ручка уже находится в использовании, то начинайте использование с пункта «Установка дозы». |
| 9. Удерживая шприц-ручку иглой вверх, нажимайте на пусковую кнопку и удерживайте ее в этом положении, cелектор дозировки издаст щелчок, в дозировочном окне появится значение ноль «0». На конце иглы должна появиться 1 (2) капля препарата. | 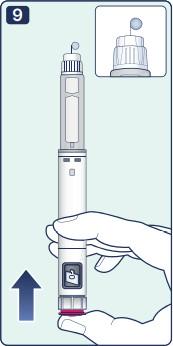
|
|
Если после проверки прохождения (поступления) препарата капля не появилась на конце иглы, необходимо повторить действия пункта «II», но не более 6 раз. Если капля препарата так и не появилась, необходимо заменить иглу и повторить действия пункта
«II» Проверка прохождения (поступления) препарата через иглу» еще раз. Если капля раствора так и не появилась, необходимо утилизировать шприц-ручку и использовать новую.
Перед использованием шприц-ручки в первый раз следует быть уверенным в том, что игла хорошо пропускает препарат, а на конце иглы появилась капля раствора. Это гарантирует введение препарата. Если игла повреждена или закупорена, капля раствора не появится, препарат не будет введен, даже если селектор дозировки и счетчик дозы будут двигаться. Пациент может не ввести необходимую дозу, и эффект препарата Семавик® Некст не будет достигнут. Необходимо обязательно проверять прохождение препарата через иглу перед первой инъекцией. |
|
| III. Установка дозы | |
|
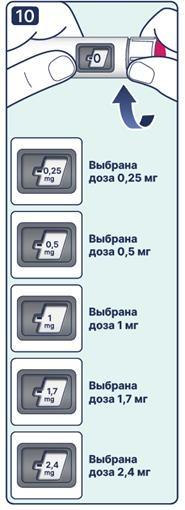
Перед каждой инъекцией необходимо проверять, какую дозу препарата (мг) пациент набрал по счётчику дозы и указателю дозы. Не ориентируйтесь на щелчки шприц- ручки, не следует их считать. На каждой шприц-ручке Семавик® Некст можно выбрать только одну дозу: 0,25 мг, или 0,5 мг, или 1 мг, или 1,7 мг, или 2,4 мг. Выбор осуществляется селектором дозы. При правильном наборе дозы счётчик дозы и указатель дозы покажут «-0,25 mg», «-0,5 mg», «-1 mg», «-1,7 mg», «-2,4 mg», что соответствует выбранной дозе 0,25 мг, 0,5 мг, 1 мг, 1,7 мг и 2,4 мг. |
|
|
10. Поворачивайте селектор дозы до тех пор, пока он не покажет необходимый индикатор «-0,25 mg», «-0,5 mg», «-1 mg», «-1,7 mg», «-2,4 mg», соответствующий дозе 0,25 мг, 0,5 мг, 1 мг, 1,7 мг и 2,4 мг. Выбранный индикатор дозы должен находиться точно напротив указателя дозы. Примечание: Если доза была выбрана неправильно, поворотным движением селектора дозы вперед или назад, установите правильную дозу. |
| 11. Для определения остаточного количества препарата, необходимо использовать счётчик дозы: поворачивая селектор дозы до остановки счетчика дозы. Если в дозировочном окне он показывает «-0,25 mg», или «-0,5 mg», или «-1 mg», или «-1,7 mg», или «-2,4 mg», в шприц-ручке осталось не менее указанной дозы. Если счётчик дозы остановился до того, как появилось «- 0,25 mg», или «-0,5 mg», или «-1 mg», или «-1,7 mg», или «-2,4 mg», то это означает, что в шприц-ручке осталось недостаточное количество препарата, чтобы ввести полную дозу. | 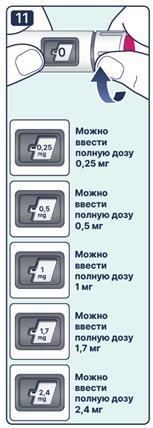
|
| Важно! Не используйте шприц-ручку, если осталось недостаточное количество препарата для введения полной дозы. Используйте новую шприц-ручку. | |
| IV. Введение препарата | |
|
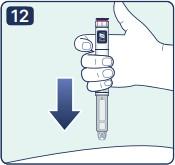
12. Одним непрерывным движением руки введите иглу под кожу. Примечание: Используйте техники инъекций, рекомендованные врачом или средним медицинским персоналом. |
|
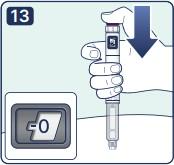
13. Убедитесь, что дозировочное окно находится в поле зрения человека, проводящего инъекцию. Нажмите на пусковую кнопку и удерживайте ее, пока значение «0» не совпадет с указателем дозы. При нажатии на кнопку пациент может услышать или ощутить щелчок. Нельзя дотрагиваться пальцами до счетчика дозы в дозировочном окне - это может прервать инъекцию |
|
|
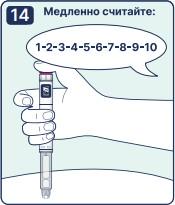
14. Удерживайте иглу под кожей, после того, как счетчик дозы вернулся к «0» и медленно считайте до 6. Примечание: Если извлечь иглу из-под кожи раньше, пациент может увидеть, как препарат вытекает из иглы. В этом случае будет введена неполная доза препарата. |
|
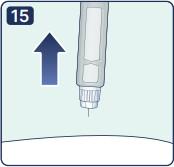
15. Осторожно извлеките иглу из-под кожи. Примечание: Если в месте инъекции появилась кровь, необходимо слегка прижать к месту укола ватный тампон. Не следует массировать место укола. После завершения инъекции пациент может увидеть каплю раствора на конце иглы. Это нормально и не влияет на дозу препарата, которая введена. |
|
| V. Утилизация иглы | |
|
Важно! После каждой инъекции препарата всегда удаляйте иглу со шприц-ручки. Это может предотвратить закупорку игл, загрязнение, инфицирование, вытекание раствора и введение неправильной дозы препарата. Хранить и транспортировать шприц-ручку необходимо без иглы! |
|
|
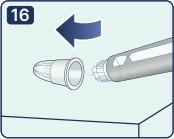
16. После завершения инъекции осторожно наденьте внешнюю насадку на иглу до упора. |
|
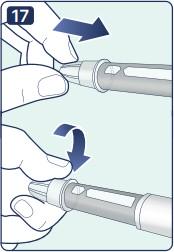
17. Открутите иглу и выбросите ее вместе с внешней насадкой, соблюдая меры предосторожности. Примечание: При утилизации использованных игл соблюдайте местные требования, нормы и правила обращения с потенциально инфицированными материалами. |
|
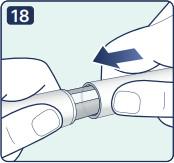
|
18. Наденьте колпачок шприц-ручки и храните шприц-ручку до следующего использования согласно условиям хранения, указанным в инструкции по применению препарата. |
| VI. Уход за шприц-ручкой | |
|
Со шприц-ручкой следует обращаться аккуратно. Небрежное или неправильное обращение может стать причиной неправильной дозировки препарат Семавик® Некст, что может привести к слишком высокой или слишком низкой концентрации глюкозы крови или вызвать дискомфорт в области живота (тошнота или рвота). Необходимо предохранять шприц-ручку от попадания пыли, загрязнений и жидкости. Запрещается мыть шприц-ручку, погружать ее в жидкости. По мере загрязнения шприц-ручку можно протирать влажной тканью, смоченной мягким моющим средством. Если шприц-ручка подверглась физическому воздействию (удар, механическая вибрация, термические явления и пр.) или пациент сомневается в ее исправности, необходимо присоединить новую иглу и проверить прохождение (поступление) препарата перед тем, как сделать инъекцию. Запрещается оставлять шприц-ручку в местах, где она может подвергаться воздействию слишком высоких или слишком низких температур (в автомобиле, на подоконнике и пр.). Запрещается проводить инъекцию препарат Семавик® Некст, если он был заморожен. Использованную (пустую) шприц-ручку необходимо выбросить. Выбрасывать пустую шприц-ручку с отсоединенной иглой необходимо в соответствии с рекомендациями, данными врачом, медсестрой, фармацевтом или местными требованиями. |
|
Пен-иньектор представляет собой предварительно заполненную одноразовую шприц-ручку для многократных инъекций (далее «Шприц-ручка»), содержащую гипогликемическое средство, аналог глюкагоноподобного пептида-1 (ГПП-1) – семаглутид.
На данный момент в РФ представлены 2 шприц-ручки Семавик® Некст: одна с дозой 1,7 мг, другая - с дозой 2,4 мг. Они продаются в разных упаковках и позволяют сделать инъекцию только в указанной на этикетке дозировке. Шприц-ручки Семавик® Некст не содержат делений с дозами 0,25 мг, 0,5 мг и 1 мг, как у препарата Семавик®.
При наборе дозы препарата Семавик® Некст не рекомендуется ориентироваться на щелчки и взаимозаменять шприц-ручки. Это связано с тем, что шприц-ручки с различными дозами препарата Семавик® Некст содержат разные концентрации семаглутида. Использование шприц-ручки с несоответствующей дозой может привести к ошибкам при введении – недостаточному или избыточному количеству препарата, снизить его эффективность и вызвать серьезные последствия для здоровья.

